化合物スクリーニングで期待された効果を示す化合物を特定するAIモデル 京都大学が開発:「既存の治療薬よりも効果がある化合物が見つかった」
京都大学のiPS細胞研究所は、AIを活用した創薬に向けて熱拡散方程式を応用した新たなアルゴリズムを開発した。ALS患者のiPS細胞を使って化合物の学習やスクリーニングを実施したところ、既存薬よりも高い効果を示す化合物を同定できた。
この記事は会員限定です。会員登録(無料)すると全てご覧いただけます。
京都大学のiPS細胞研究所は2020年11月12日、AI(人工知能)を活用した創薬に向けて新たなアルゴリズムを開発し、既存薬よりも高い効果を示す化合物を同定できたと発表した。
開発したのは、化合物スクリーニングで期待された効果を示す化合物を予測する「熱拡散方程式」(HDE)モデル。このモデルは、熱が拡散していく様子を模して化合物の有効性の高さをスコア化することで、期待される効果を示した化合物を予測する。
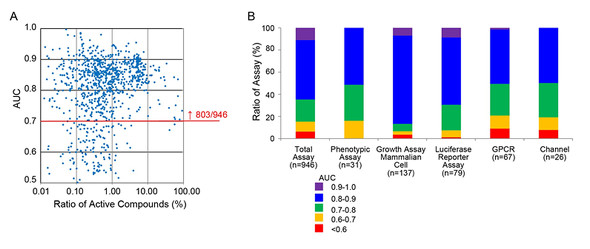
一般公開されている化合物スクリーニングのデータベース(PubChem)を使って、HDEモデルの予測精度を評価した。946セットのデータベースを評価したところ、803セットで0.7以上のAUC(機械学習の評価指標。1に近いほど判定能力が高い)を示したという。
既存の治療薬よりも効果がある化合物を特定
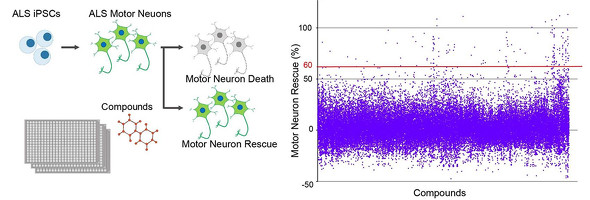
ALS(筋萎縮性側索硬化症)患者のiPS細胞から作製した約5万個の運動神経細胞を使って、細胞死を抑制する化合物のスクリーニングを実施した。細胞死抑制率60%をしきい値として、期待される効果を示す化合物を求めた。その結果をHDEモデルに学習させ、約200万個の化合物の有効性を予測したところ、5875個の化合物を抽出した。
抽出したこれらの化合物について、約30株のALS患者のiPS細胞から作製した運動神経細胞で評価したところ、ALSの治療薬として認可されている「リルゾール」や「エダラボン」よりも細胞死抑制効果が強く、多くのALS患者運動神経細胞に効果を示す化合物を同定できた。これらの化合物は、未知の化合物の特徴を有しており、ALSに対する新たな薬剤開発のシーズとして利用されることになったとしている。
関連記事
 AI教育助手に要求される性質は何か、米大学研究者の調査で明らかに
AI教育助手に要求される性質は何か、米大学研究者の調査で明らかに
セントラルフロリダ大学の研究者は、オンライン教育などで導入され始めているAIベースの教育助手が役立つかどうかを決めるのはどのような要素なのかを調査した。その結果、有能さ以外にもう一つの要因があることが分かった。 「世界のAI支出額は今後4年間で倍増する」 IDCが予測
「世界のAI支出額は今後4年間で倍増する」 IDCが予測
IDC Japanは、世界のAIの支出額に関する予測を発表した。2019〜2024年の年間平均成長率を20.1%と見込み、支出額は2020年の501億ドルから2024年には1100億ドル以上になると予測する。 AIで「発作がまだ起きていない」心房細動を予測 カルディオインテリジェンスが治験を実施
AIで「発作がまだ起きていない」心房細動を予測 カルディオインテリジェンスが治験を実施
カルディオインテリジェンスは、国立研究開発法人日本医療研究開発機構(AMED)が公募した「医療機器開発推進研究事業」に採択され、ディープラーニングを活用した隠れ心房細動診断の治験を実施する。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.