曌嫮夛偱柧傜偐偵側偭偨堛椕岦偗OSS偺懡條側妶梡朄劅劅揹巕僇儖僥丄椪彴帋尡僨乕僞夝愅丄擔杮岅堛妛梡岅僾儔僢僩僼僅乕儉丄夋憸DB丗僿儖僗働傾偩偗偱廔傢傜偣側偄堛椕IT乮6乯乮2/4 儁乕僕乯
亂R偲CDISC亃OSS偩偗偱岠棪揑側椪彴僨乕僞夝愅偑壜擻側帪戙偵
丂搶嫗戝妛 UMIN僙儞僞乕乮戝妛昦堾堛椕忣曬僱僢僩儚乕僋尋媶僙儞僞乕乯偺壀揷徆巎巵偑乽R偲CDISC乿偲戣偟偰峴偭偨曬崘偱偼丄椪彴帋尡偺僨乕僞夝愅偑丄崙嵺昗弨偵弨嫆偟偨儊僞僨乕僞偲僨乕僞僙僢僩傪梡偄傞偙偲偵傛偭偰丄OSS僣乕儖乮摑寁夝愅梡僾儘僌儔儈儞僌娐嫬偺R偲丄偦偺僷僢働乕僕乯偩偗傪巊偭偰岠棪揑偵幚尰偱偒傞帪戙偑摓棃偟偨偙偲偑柧傜偐偵偝傟偨丅
丂OSS偵傛傞杮奿揑側夝愅側壜擻偵側偭偨攚宨偵偼丄堛妛椞堟偱偺椪彴僨乕僞岎姺偺婯奿偱偁傞乽CDISC乮Clinical Data Interchange Standards Consortium乯乿昗弨偺僆乕僾儞壔偑偁傞丅CDISC昗弨偼丄偙傟傑偱ODM乮Operational Data Model乯儀乕僗偺XML偵傛傞儊僞僨乕僞偺昞尰乮Define-XML乯偵偼懳墳偟偰偄偨偑丄僨乕僞偦偺傕偺偺昞尰偵偮偄偰偼XML偵懳墳偟偰偍傜偢丄摿掕偺夝愅僣乕儖儀儞僟乕偺僨乕僞昞尰偩偗偵懳墳偟偰偄偨丅偦偺偨傔丄OSS僣乕儖偲偺楢実傪廫暘偵恾傞偙偲偼偱偒側偐偭偨丅
丂偟偐偟丄2014擭偵CDISC昗弨偑XML偵傛傞僨乕僞昞尰偵惓幃偵堏峴偟偨偙偲偵傛偭偰丄R側偳偺OSS僣乕儖偱偺棙梡偑壜擻偵側偭偨丅偦偺寢壥偲偟偰丄乽OSS僣乕儖偩偗偱丄崙嵺昗弨宍幃偺儊僞僨乕僞傪敽偭偨椪彴帋尡僨乕僞僙僢僩傪嶌惉偟丄岠棪揑偱儈僗偺側偄夝愅傗専嵏傪幚巤偱偒傞傛偆偵側偭偨乿偲壀揷巵偼愢柧偡傞丅
僆乕僾儞壔偱栶妱傪憹偡CDISC昗弨
丂CDISC昗弨偼丄椪彴帋尡偑巒傑偭偰偐傜廔傢傞傑偱偺丄帋尡寁夋丄僨乕僞偺廂廤丄僋儕乕僯儞僌丄僨乕僞儀乕僗傊偺拁愊丄暘愅丄儕億乕僩側偳偺婯奿傪曪娷偟偰偄傞丅偙傟傜偺婯奿偼丄乽Controlled Terminology乿偲屇偽傟傞摑惂梡岅帿彂偵傛偭偰岅渂偺摑堦偑恾傜傟偰偄傞丅
丂CDISC昗弨偼丄暷崙偱偼偡偱偵丄FDA乮暷崙怘昳堛栻昳嬊乯偑惓幃偵嵦梡偟偰偍傝丄擔杮偱傕丄PMDA乮堛栻昳堛椕婡婍憤崌婡峔乯偑丄2016擭搙偐傜丄堛栻昳偺惢憿彸擣怽惪傪峴偆嵺偵丄椪彴帋尡僨乕僞傪丄CDISC昗弨偺怽惪椪彴帋尡僨乕僞儌僨儖乽SDTM乮Study Data Tabulation Model乯乿偍傛傃怽惪摑寁夝愅僨乕僞儌僨儖乽ADaM乮Analysis Data Model乯乿偵弨嫆偟偨宍幃偱採弌偡傞偙偲傪媊柋晅偗傞偲敪昞偟偰偄傞丅
丂椪彴帋尡偺悽奅偱丄CDISC昗弨偼側偤偙偺傛偆偵拲栚偝傟偰偄傞偺偐丅偦傟偼丄椪彴僨乕僞偺撪梕傪昞偡儊僞僨乕僞偑昗弨壔偝傟偰偍傝丄傛偆傗偔XML偱婰弎偝傟傞傛偆偵側偭偨偐傜偩丅偙偺儊僞僨乕僞傪巊偊偽丄摑寁夝愅僜僼僩帺恎偑彑庤偵椪彴僨乕僞偺撪梕傪夝庍偟丄夝愅張棟傪帺摦壔偱偒傞丅壀揷巵偼丄乽夝愅偱堦斣戝曄側晹暘偼丄僨乕僞偺帩偮乬抣乭偵懳墳偡傞乬堄枴乭丄偡側傢偪儊僞僨乕僞傪夝愅幰偑棟夝偡傞偙偲偩乿偲巜揈偡傞丅
丂椪彴僨乕僞儀乕僗偼昞偲偟偰昞尰偱偒丄儊僞僨乕僞偼Define-XML偲偟偰掕媊偝傟傞丅偙偺儊僞僨乕僞偵偼丄僨乕僞僙僢僩慡懱偵偳偺傛偆側昞偑娷傑傟偰偄傞偺偐傪帵偡乽Dataset-Level Metadata乿丄偦傟偧傟偺昞偵偳偺傛偆側楍偑娷傑傟偰偄傞偺偐傪帵偡乽Variable-Level Metadata乿丄偦傟偧傟偺楍偵偳偺傛偆側抣偑娷傑傟偰偄傞偺偐傪帵偡乽ValueLevel Metadata乿偑偁傞丅偦偟偰丄椪彴僨乕僞儀乕僗偦偺傕偺偼丄儊僞僨乕僞偲懳偵側偭偰丄Dataset-XML偲偟偰XML偱昞尰乮僔儕傾儔僀僘乯偝傟傞丅
R偑摑寁夝愅僜僼僩偺僨僼傽僋僩僗僞儞僟乕僪偵
丂CDISC昗弨偺僆乕僾儞壔偵傛偭偰丄椪彴帋尡偺悽奅偱傕丄傛傝懡偔偺椞堟偱OSS傪妶梡偱偒傞傛偆偵側偭偰偒偨丅拞偱傕椪彴僨乕僞傪夝愅偡傞OSS偲偟偰桳椡側偺偑GNU僾儘僕僃僋僩偺堦偮偲偟偰奐敪偑恑傔傜傟偰偄傞摑寁夝愅僾儘僌儈儔儞僌娐嫬偺R偱偁傞丅壀揷巵偼丄乽悽奅拞偺R媄弍幰偑奐敪偟偨婡擻奼挘壜擻側R僷僢働乕僕偺悢偼偙偺悢擭偱媫寖偵憹戝偟偰偍傝丄2015擭7寧尰嵼偱6789庬偵忋偭偰偄傞丅R偼偡偱偵摑寁夝愅僜僼僩偺僨僼傽僋僩僗僞儞僟乕僪偩偲尵偭偰傛偄乿偲嫮挷偡傞丅
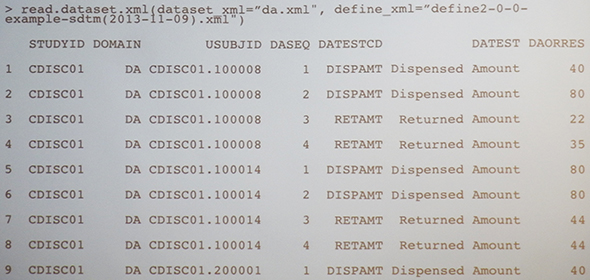
丂R僷僢働乕僕攝怣僱僢僩儚乕僋乽CRAN乮The Comprehensive R Archive Network乯乿偵搊榐偝傟偰偄傞CDISC娭楢偺R僷僢働乕僕偲偟偰偼丄ODM僼傽僀儖傪曄姺偡傞乽ODMConverter乿傗丄ODM宍幃偺堛椕宍懺傪斾妑偡傞乽CompareODM乿丄CDISC僨乕僞僼傽僀儖傪R4偵撉傒崬傑偣傞乽R4CDISC乿偑偁傞丅壓恾擇偮偼丄R4CDISC傪巊偭偰Define-XML傪R偵撉傒崬傑偣偰Dataset Level Metadata偍傛傃Variable Level Metadata傪拪弌偟偨椺傪帵偟偰偄傞丅
丂傑偨丄壓恾偵傛傞偲丄Dataset-XML傪偦偺傑傑僨乕僞僼儗乕儉偵曄姺偱偒傞偙偲偑暘偐傞丅
丂偙偺懠偵丄CDISC偵娭學偡傞OSS偲偟偰偼丄SDTM丄AdAM側偳偺僨乕僞僙僢僩偑昗弨偵揔崌偟偰偄傞偐偳偆偐傪僠僃僢僋偡傞僶儕僨乕僔儑儞僣乕儖乽OpenCDISC乿丄僨乕僞擖椡梡偺揹巕徢椺曬崘彂偺奐敪丒塣梡僣乕儖乽OpenClinica乿偑偁傞丅OpenClinica偼丄GitHub忋偱奐敪偑峴傢傟偰偍傝丄ODM偱偺僨乕僞弌椡偵懳墳偟偰偄傞丅
娭楢婰帠
 Apple Watch傗僎僲儉夝愅偲傕楢実乗乗乽僋儔僂僪宆揹巕僇儖僥乿傪僾儔僢僩僼僅乕儉偲偡傞怴偟偄乽堛椕乿偺壜擻惈
Apple Watch傗僎僲儉夝愅偲傕楢実乗乗乽僋儔僂僪宆揹巕僇儖僥乿傪僾儔僢僩僼僅乕儉偲偡傞怴偟偄乽堛椕乿偺壜擻惈
擔杮偱峔抸偑媫偑傟偰偄傞乽抧堟曪妵働傾僔僗僥儉乿偺廳梫側婎斦偲峫偊傜傟偰偄傞乽揹巕僇儖僥乿僔僗僥儉丅僋儔僂僪宆揹巕僇儖僥偑堛椕僨乕僞拁愊偺偨傔偺僾儔僢僩僼僅乕儉偲側傞偙偲偵傛傝丄堛椕偦偺傕偺偺恑壔傪屻墴偟偡傞壜擻惈傕惗傑傟偰偄傞偲偄偆丅 Watson偼僗儅乕僩僼僅儞乛僂僃傾儔僽儖抂枛偱廂廤偟偨儐乕僓乕僨乕僞偺妶梡偱堛椕IT傪妚怴偱偒傞偺偐
Watson偼僗儅乕僩僼僅儞乛僂僃傾儔僽儖抂枛偱廂廤偟偨儐乕僓乕僨乕僞偺妶梡偱堛椕IT傪妚怴偱偒傞偺偐
乽IBM Watson乿偼丄僗儅乕僩僼僅儞傗僂僃傾儔僽儖抂枛側偳偺僨僶僀僗偐傜廂廤偟偨僨乕僞偲丄揹巕僇儖僥傗堚揱巕忣曬側偳偺朿戝側堛椕忣曬偲傪桳婡揑偵寢傃晅偗偰堛椕尰応偺妶摦傪巟墖偱偒傞擣抦僔僗僥儉偲偟偰拲栚傪廤傔偰偄傞丅杮峞偱偼丄2015擭5寧19擔丄20擔偵搶嫗偱奐嵜偝傟偨乽IBM XCITE SPRING 2015乿偱偺島墘撪梕傪婎偵丄IBM Watson偑偳偺傛偆偵恑壔偟丄堛椕傗儔僀僼僒僀僄儞僗暘栰偱妶梡偝傟傛偆偲偟偰偄傞偺偐傪徯夘偡傞丅 僗儅乕僩僨僶僀僗偐傜偺儘僌丄昦堾DB丄堛椕婡婍偐傜摼傞夋憸乗乗堛椕尰応偺價僢僌僨乕僞妶梡傪幚慔偡傞3幮偺帠椺
僗儅乕僩僨僶僀僗偐傜偺儘僌丄昦堾DB丄堛椕婡婍偐傜摼傞夋憸乗乗堛椕尰応偺價僢僌僨乕僞妶梡傪幚慔偡傞3幮偺帠椺
堛椕丄僿儖僗働傾偵娭楢偟偨僥僋僲儘僕價僕僱僗傗僗僞乕僩傾僢僾偺摦岦傪丄僄儞僕僯傾傗價僕僱僗儅儞偵懳偟偰徯夘偡傞僀儀儞僩乽Digital Health Meetup Vol.2乿偺僺僢僠僙僢僔儑儞偐傜3幮偺堛椕儀儞僠儍乕偑奐敪偟偨僒乕價僗傗傾僾儕偺帠椺傪偍揱偊偡傞丅 尰栶堛巘傗堛椕儀儞僠儍乕偑岅傞丄堛巘夛丄IT妶梡丄挻崅楊幰丄偦偟偰枹棃傊
尰栶堛巘傗堛椕儀儞僠儍乕偑岅傞丄堛巘夛丄IT妶梡丄挻崅楊幰丄偦偟偰枹棃傊
堛椕丄僿儖僗働傾偵娭楢偟偨僥僋僲儘僕價僕僱僗傗僗僞乕僩傾僢僾偺摦岦傪丄僄儞僕僯傾傗價僕僱僗儅儞偵懳偟偰徯夘偡傞僀儀儞僩乽Digital Health Meetup Vol.2乿偺僷僱儖僨傿僗僇僢僔儑儞乽堛椕妚柦両 堛巘偺IT妶梡偲偦偺枹棃偵偮偄偰乿偺柾條傪偍揱偊偡傞丅 2025擭栤戣丄儅僀僫儞僶乕丄夵惓栻帠朄乗乗奐敪幰偑乽桞堦偺惉挿巗応乿僿儖僗働傾乛堛椕偵嶲擖偡傞嵺偺壽戣偲偼
2025擭栤戣丄儅僀僫儞僶乕丄夵惓栻帠朄乗乗奐敪幰偑乽桞堦偺惉挿巗応乿僿儖僗働傾乛堛椕偵嶲擖偡傞嵺偺壽戣偲偼
堛椕丄僿儖僗働傾偵娭楢偟偨僥僋僲儘僕價僕僱僗傗僗僞乕僩傾僢僾偺摦岦傪丄僄儞僕僯傾傗價僕僱僗儅儞偵懳偟偰徯夘偡傞僀儀儞僩乽Digital Health Meetup Vol.2乿偺島墘乽堛椕惌嶔偺摦岦偐傜撉傒夝偔丄偙傟偐傜偺堛椕丒夘岇嬈奅乿偺柾條偐傜僿儖僗働傾乛堛椕嬈奅偵墶偨傢傞壽戣傪傑偲傔偰偍揱偊偡傞丅 堛椕亊IT丂堛巘偼僾儘僌儔儈儞僌偱堛椕偺巇慻傒傪曄偊傜傟傞偐
堛椕亊IT丂堛巘偼僾儘僌儔儈儞僌偱堛椕偺巇慻傒傪曄偊傜傟傞偐
僾儘僌儔儈儞僌偼僾儘僌儔儅乕偩偗偺摿尃偱偼側偄丠乗乗IT傪妶梡偟偰帺恎偺愱栧暘栰傪傛傝椙偔偟偰偄偙偆偲僠儍儗儞僕偟偰偄傞恖偨偪偵偍榖傪巉偆僀儞僞價儏乕僔儕乕僘丄杮擔巒摦丅 傾僢僾儖偑GitHub偵岞奐偟偨堛椕偺尋媶挷嵏梡OSS僼儗乕儉儚乕僋乽ResearchKit乿偺婎慴抦幆
傾僢僾儖偑GitHub偵岞奐偟偨堛椕偺尋媶挷嵏梡OSS僼儗乕儉儚乕僋乽ResearchKit乿偺婎慴抦幆
暷傾僢僾儖偑2015擭4寧14擔偵GitHub偵岞奐偟偨堛椕偺尋媶挷嵏梡OSS僼儗乕儉儚乕僋乽ResearchKit乿偵偮偄偰丄奣梫傗婡擻丄尰帪揰偱偱偒側偄偙偲丄偳偺傛偆側傾僾儕偑嶌傟傞偐偵偮偄偰徯夘偡傞丅 堛幰偼IT媄弍傪妛傃丄僄儞僕僯傾偼堛妛傪妛傇帪戙
堛幰偼IT媄弍傪妛傃丄僄儞僕僯傾偼堛妛傪妛傇帪戙
2013擭8寧31擔丄乽10擭屻偺堛椕乿傪僥乕儅偵擔杮奺抧偐傜1000恖偺堛妛惗偑搒撪偵廤寢丅乽Medical Future Fes 2013乿偑奐嵜偝傟偨丅
Copyright © ITmedia, Inc. All Rights Reserved.

 搶嫗戝妛 UMIN僙儞僞乕乮戝妛昦堾堛椕忣曬僱僢僩儚乕僋尋媶僙儞僞乕乯 壀揷徆巎巵
搶嫗戝妛 UMIN僙儞僞乕乮戝妛昦堾堛椕忣曬僱僢僩儚乕僋尋媶僙儞僞乕乯 壀揷徆巎巵
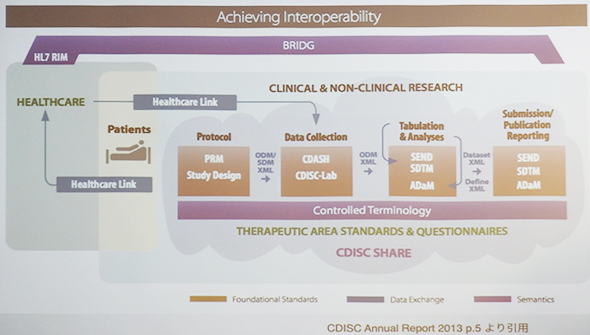
 夝愅偲儊僞僨乕僞乮壀揷巵偺島墘帒椏傛傝乯
夝愅偲儊僞僨乕僞乮壀揷巵偺島墘帒椏傛傝乯